
Kurzzusammenfassung
Ein Verständnis für den Einfluss atmosphärischer Bedingungen auf die Überlebensfähigkeit luftgetragener Mikroorganismen ist unabdingbar für den Versuch, die Epidemiologie von über die Luft übertragenen Infektionen zu formulieren. Der Einfluss der relativen Luftfeuchtigkeit ist bisher nur unzureichend quantitativ untersucht worden, und ihr wurden widersprüchliche Effekte zugewiesen hinsichtlich der Frage, ob sie dem Überleben luftgetragener Pathogene zuträglich ist oder es zerstört. Williamson und Gotaas (1) folgerten aus ihren Beobachtungen zu Serratia marcescens, Escherichia coli, Staphylococcus albus, Staphylococcus aureus und Streptococcus salivarius, dass eine niedrige relative Luftfeuchtigkeit das Überleben von Luftkeimen eher fördert als eine hohe.
Ganz ähnlich berichteten Edwards et al. sowie Loosli und seine Mitarbeiter (2), dass dispergierte Influenzaviren in feuchter Luft schneller zugrunde gehen als in trockener, und DeOme (3) fand heraus, dass die Sterberate von aus wässriger Suspension zerstäubten Salmonella pullorum mit zunehmender relativer Luftfeuchtigkeit von 15 auf 80 Prozent kontinuierlich ansteigt. Wells und Zappasodi (4) dagegen stellten fest, dass in die Luft gesprühte hämolytische Streptokokken in trockenen Bedingungen rasch absterben, in Anwesenheit von Feuchtigkeit dagegen geschützt sind.
In nur wenigen dieser Untersuchungen wurden wirklich zahlreiche, mit der relativen Luftfeuchtigkeit verbundene Punkte untersucht, und in einigen Fällen wurden auch nicht die genauen Werte des atmosphärischen Feuchtigkeitsgehalts bestimmt. Der beträchtliche Einfluss von Wasserdampf auf die Wirkung luftgebundener Germizide (5, 6) macht eine sorgfältigere Untersuchung auch seiner Effekte auf Mikroorganismen wünschenswert.
In der vorliegenden Studie wurden bakterielle Suspensionen in einer Versuchskammer unter kontrollierten Bedingungen hinsichtlich Temperatur und relativer Luftfeuchtigkeit zerstäubt. Die Konzentration überlebender Mikroorganismen in der Luft wurde nach verschiedenen Zeitintervallen gemessen.
Studie von Edward W. Dunklin und Theodore T. Puck
Methoden
Die Experimente wurden in zuvor beschriebenen (7) 18 Kubikmeter großen Kammern durchgeführt, welche die präzise Kontrolle von Temperatur und relativer Luftfeuchtigkeit über einen recht weiten Bereich ermöglichen.Siebeneinhalbstündige Kulturen von Mikroorganismen wurden in einem Herz-Nährmedium (Difco) mit zugesetztem Serum und mit Dextrose herangezüchtet. Aus diesen Kulturen hergestellte Suspensionen wurden unter Anwendung der bereits beschriebenen Standardtechnik (7) eine Minute lang in die Versuchskammern zerstäubt. Die bakteriellen Suspensionen wurden mithilfe refluxbasierter Zerstäuber (8) dispergiert, deren Partikelgrößenverteilung mit einem Kaskadenimpaktor1 (9) gemessen wurde.
Durch die sorgsame Standardisierung des Sprühverfahrens war es möglich, in jedem Experiment eine jeweils konstante Zahl von Mikroorganismen in die 18 Kubikmeter große Kammer einzubringen. Diese Zahl wurde auf ca. 5 Millionen festgelegt. Die Gesamtzahl der durch den Zerstäuber ausgestoßenen Mikroorganismen wurde täglich überprüft, indem der Zerstäuber direkt an einen Bubbler Sampler (10, ein Luftprobenehmer) angeschlossen und dann das Sprühverfahren durchgeführt wurde, sodass das gesamte Aerosol von der Bubbler-Flüssigkeit absorbiert wurde. Aliquote davon wurden dann auf Nähragar ausplattiert. Der Bakteriengehalt der Luft wurde über einen Zeitraum von zwei Stunden nach der Zerstäubung der Mikroorganismen bestimmt, indem fortlaufend alle zwei Minuten eine Bubbler-Probe genommen wurde und Agarplatten zum Absetzen von Mikroorganismen bereitgestellt wurden (7).
| Probezeitpunkt (Intervall zwischen Beendigung des Sprühvorgangs und Beginn der Probenahme) in Minuten |
Anzahl Pneumokokken pro Kubikfuß Luft, gewonnen mit dem Bubbler Sampler | Anzahl Pneumokokken auf einer 5 Minuten lang aufgestellten Absetzplatte |
|---|---|---|
| 0 | 5 200 | 332 |
| 5 | 4 580 | 290 |
| 10 | 4 000 | 247 |
| 20 | 3 800 | 193 |
| 30 | 3 240 | 177 |
| 45 | 2 700 | 152 |
| 60 | 2 420 | 106 |
| 75 | 2 240 | 96 |
| 90 | 1 940 | 90 |
| 105 | 1 800 | 74 |
| 120 | 1 620 | 66 |
Tabelle 1
Überleben von Pneumokokken Typ I, aus Suspension in Nährmedium in die Luft gesprüht, bei einer Temperatur von 22,2°C und einer relativen Luftfeuchtigkeit von 19 Prozent Der mediane Massendurchmesser des aus dem Zerstäuber austretenden bakteriellen Sprühnebels lag bei 3,2 µm
Die mittels dieser zwei Testmethoden ermittelten Überlebenskurven verliefen parallel zueinander. Insgesamt waren die mit dem Bubbler Sampler ermittelten Werte etwas einheitlicher, weshalb diese für die Berechnungen der Überlebenskonstanten herangezogen wurden, die hier nachfolgend dargestellt werden. Tabelle I zeigt ein typisches Versuchsprotokoll.
Die relative Luftfeuchtigkeit wurde über einen Bereich zwischen 3 und 80 Prozent bei drei verschiedenen Temperaturen, 14,4, 22,2 und 33,3°C, variiert. Für die Temperatur- und Luftfeuchtigkeitsbereiche mit sehr hohen bakteriellen Sterberaten wurden die Ergebnisse durch viele Wiederholungen jedes Experiments überprüft.
Versuchsergebnisse
Das bemerkenswerteste Ergebnis dieser Untersuchungen war die Demonstration der Existenz eines engen Bereichs relativer Luftfeuchtigkeit nahe 50 Prozent, der für Bakterien, die aus einer Suspension im Nährmedium frisch in die Luft gesprüht wurden, rasch letal wirkt.Der Pneumokokkus, ein relativ empfindlicher Mikroorganismus, erwies sich als am anfälligsten für diese tödliche Wirkung der Atmosphäre, während der Effekt beim Streptokokkus Gruppe C und beim Staphylokokkus weit weniger ausgeprägt war. In Abb. 1 sind typische Ergebnisse eines Experiments mit Pneumokokken bei drei verschiedenen relativen Luftfeuchtigkeiten dargestellt, welche die Fähigkeit des Mikroorganismus demonstrieren, sowohl bei sehr niedrigen als auch bei sehr hohen relativen Luftfeuchtigkeiten über längere Zeiträume zu überleben, nicht aber bei mittleren Werten.
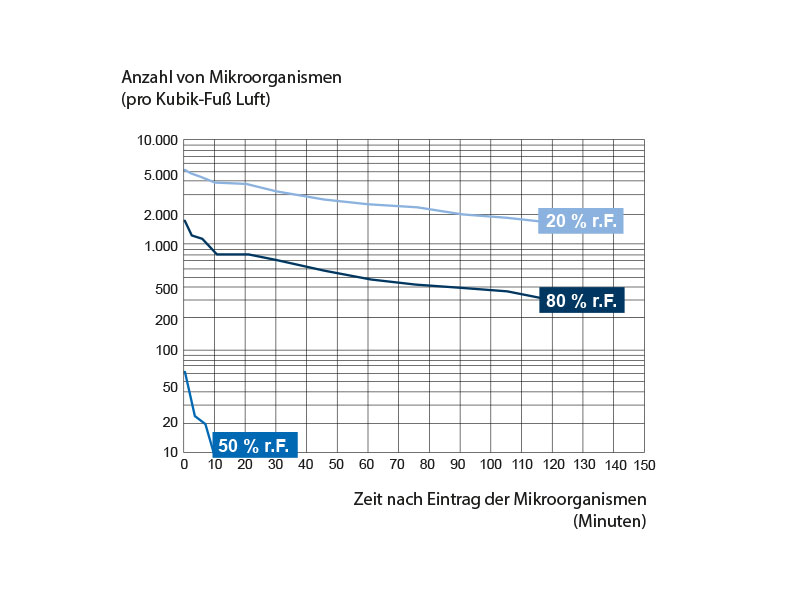
Logarithmische Darstellung des Überlebens von aus Nährkultur in die Atmosphäre gesprühten Pneumokokken bei verschiedenen relativen Luftfeuchtigkeiten und 22,2°C. Die aus dem Zerstäuber austretende Wolke hatte einen medianen Massendurchmesser von 3,2 µm. In jedem Experiment wurde eine ungefähr gleiche Zahl von Mikroorganismen in die Kammer eingebracht.
Die Analyse der Überlebenskurven zeigt, dass mindestens zwei unabhängige letale Prozesse involviert sind, die die Rate beeinflussen. Der erste Prozess erfolgt stets sehr rapide und sorgt zwischen Minute 5 und Minute 20 nach Einbringen der Tröpfchen mit Mikroorganismen in die Luft für ein ausgeprägtes Absterben. Der zweite Zerfallsprozess schreitet langsamer voran und erstreckt sich im Allgemeinen über den gesamten zweistündigen Beobachtungszeitraum (Abb. 1).
Beide Sterbeprozesse ergeben lineare logarithmische Überlebenskurven, sodass beim Auftragen der Anzahl überlebender Keime als logarithmische Funktion der Zeit die resultierende Kurve aus zwei geraden Linien besteht, die sich an einem Punkt zwischen 5 und 20 Minuten nach Einbringen der Mikroorganismen in die Kammer überschneiden. Es wurde ermittelt, dass die Steigungen dieser zwei Teile der Kurve von der relativen Luftfeuchtigkeit und der Temperatur, der Natur der eingesetzten Mikroorganismen, der Zusammensetzung des flüssigen Mediums, in dem sie suspendiert sind, und der Partikelgröße der Tröpfchen, innerhalb derer sie in die Atmosphäre eingebracht werden, beeinflusst werden. Experimentelle Effekte, die die Wirkungsweise dieser Faktoren demonstrieren, wurden am ausführlichsten für Pneumokokken untersucht.
Experimente vergleichbar mit den in Abb. 1 dargestellten wurden, stets unter Verwendung von Suspensionen siebeneinhalbstündiger Pneumokokken-Kulturen in einem Serum-Dextrose-Medium, bei vielen verschiedenen relativen Luftfeuchtigkeiten durchgeführt. Für jedes Experiment wurde die Anzahl überlebender Keime als logarithmische Funktion der Zeit aufgetragen (wie in Abb. 1 gezeigt) und Werte für die zwei Konstanten K1 und K2 (welche die logarithmischen Raten des Verschwindens lebensfähiger Mikroorganismen aus der Luft während der ersten 10 bis 15 Minuten (K1) bzw. für das darauffolgende Intervall (K>sub>2) repräsentieren) wurden bei jeder relativen Luftfeuchtigkeit bei 22,2°C ermittelt. Der in diesen Verfahren eingesetzte Zerstäuber erzeugt eine Wolke von Tröpfchen aus in dem Nährmedium suspendierten Bakterien, deren medianer Massendurchmesser2 beim Austritt aus dem Zerstäuber 3,2 µm beträgt.
Abb. 2 präsentiert eine grafische Darstellung dieser Überlebenskurven. Es zeigt sich, dass in einem engen Bereich relativer Luftfeuchtigkeit zwischen 40 und 55 Prozent die Sterberate der aus der Suspension in dem Nährmedium in die Luft gesprühten Mikroorganismen stark beschleunigt wird.
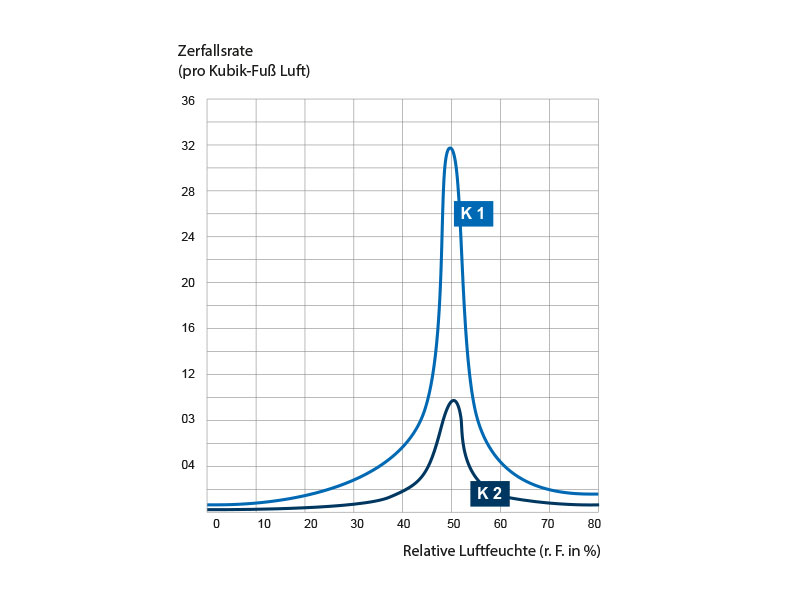
Steigungen der logarithmischen Überlebenskurven für Pneumokokken, die aus Suspension im Nährmedium in Atmosphären verschiedener relativer Luftfeuchtigkeiten gesprüht wurden. K1 ist die Steigung des ersten Teils der Überlebenskurve, K2 ist die logarithmische Zerfallskonstante für den letzten Teil der Kurve. Der Wert für K1 bei 50 Prozent relativer Luftfeuchtigkeit, 0,32 ± 0,12, ist der Mittelwert der Ergebnisse aus mehr als einem Dutzend Experimenten. Genaue Werte für K2 im mittleren Luftfeuchtigkeitsbereich konnten nicht ermittelt werden, da nur wenige Mikroorganismen länger als 20 Minuten überlebt haben.
Auswirkungen der Art von Mikroorganismus
Staphylococcus albus und Streptococcus hemolyticus Gruppe C wiesen logarithmische Überlebenskurven auf, die mit den in Abb. 1 für Pneumokokkus dargestellten vergleichbar waren. Die Auswirkungen der relativen Luftfeuchtigkeit auf die Sterberaten dieser Mikroorganismen folgten dem gleichen Muster. Als einzige Unterschiede wurden die relative Ausprägung des Effekts sowie eine leichte Verschiebung des relativen Luftfeuchtigkeitswerts mit der maximalen Sterberate beobachtet. Die Reihenfolge zunehmender Anfälligkeit für die tödliche Wirkung einer mittleren relativen Luftfeuchtigkeit war: hämolytischer Streptokokkus Gruppe C, Staphylokokkus und Pneumokokkus Typ I. Der Effekt verschiedener relativer Luftfeuchtigkeiten auf die Überlebenskonstanten von Streptokokkus und Staphylokokkus ist in Abb. 3 dargestellt.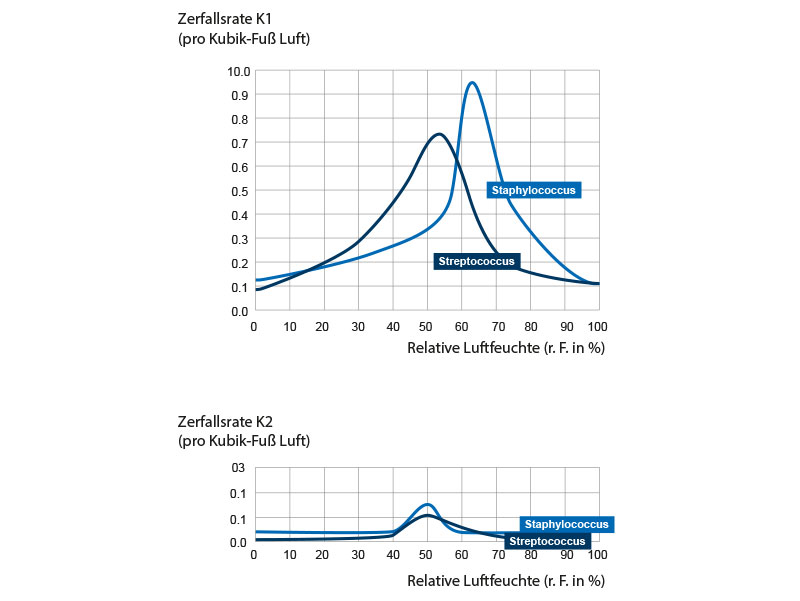
Logarithmische Zerfallskonstanten K1 und K2 des hämolytischen Streptokokkus Gruppe C und von Staphylococcus albus als Funktion der relativen Luftfeuchtigkeit. Die Mikroorganismen wurden aus der Suspension in dem Nährmedium in die Luft gesprüht.
Effekt des Absetzens
Es ist notwendig, zu ermitteln, in welchem Ausmaß das Verschwinden der Mikroorganismen aus der Luft einen wirklichen Sterbeprozess repräsentiert, im Gegensatz zur Entfernung von in der Luft befindlichen Partikeln durch Absetzen oder Koaleszenz. Um das zu untersuchen, wurde eine Versuchsreihe mit den in Abb. 2 präsentierten Bedingungen mit einer mikrobiellen Nährkultur, der Methylenblau zugesetzt wurde, wiederholt. Proben der Kammerluft wurden in den gleichen Zeitintervallen wie in den vorangegangenen Experimenten genommen und durch eine Lösung von 70% Alkohol in H2O gesprudelt. Anschließend wurde für jede dieser Proben photometrisch die Gesamtmenge angesammelten Farbstoffs bestimmt. Auf diese Weise wurde die Entfernungsrate dieser Partikel aus der Luft durch unelastische Kollisionen mit den Wänden und dem Boden der Kammer bestimmt.
Bestimmung der Absetzraten durch Messung der Persistenz von Tröpfchen mit Mikroorganismen und Farbstoff in der Luft bei verschiedenen relativen Luftfeuchtigkeiten. Das Suspensionsmedium war eine Nährlösung und der unmittelbare mediane Massendurchmesser der Wolke betrug 3,2 µm. (Die Ordinateneinheiten sind willkürlich, die Abbildungen zeigen lediglich die relativen Mengen an Farbstoff pro Kubikfuß Luft als Funktion der Zeit.)
Abb. 4 präsentiert beispielhafte Darstellungen dieser Daten. Die auf diese Weise ermittelten logarithmischen Kurven bestehen ebenfalls aus zwei geraden Linien mit einem Einschnitt üblicherweise zwischen 10 und 20 Minuten. Werden die Steigungen der Kurven jedoch wie in Abb. 5 gegen das gesamte Spektrum relativer Luftfeuchtigkeiten aufgetragen, ist weder für K1 noch für K2 ein Maximum zu beobachten, wie es bei der Gewinnung überlebender Mikroorganismen aus der Luft der Fall war. Die Absetzrate bleibt bei allen relativen Luftfeuchtigkeiten niedrig3, während die Rate des Verschwindens beispielsweise lebensfähiger Pneumokokken bei mittleren Luftfeuchtigkeiten um das 50- bis 100-Fache gesteigert sein kann. Da das rapide Verschwinden von Mikroorganismen, die aus Suspension im Nährmedium in Atmosphären mittlerer Luftfeuchtigkeiten gesprüht wurden, nicht durch das Absetzen oder Kollisionsprozesse erklärt werden kann, muss bei relativen Luftfeuchtigkeiten um 50 Prozent ein tatsächlicher letaler Vorgang stattfinden.4
Eine Erklärung für dieses rasche Absterben von Luftkeimen, das in Atmosphären mit mittleren relativen Luftfeuchtigkeiten auftritt, muss durch die Analyse der Prozesse erfolgen, die beim Einbringen von mit Bakterien beladenen Tröpfchen in ungesättigte Luft stattfinden. Die Verdunstung von Wasser aus solchen Tröpfchen resultiert zunächst in einer Steigerung der Konzentration aller in der Flüssigkeit befindlichen löslichen Substanzen, die den Mikroorganismus umgeben. Sobald genügend Wasser verloren gegangen ist, können eine oder mehrere gelöste Substanzen eine Konzentration erreichen, die auf die Zelle toxisch wirkt. Gleichzeitig verliert jedoch auch die bakterielle Zelle selbst Wasser.
Wenn die Zelle stark austrocknet, wird sie resistent gegen viele Arten physikalischer und chemischer Stressfaktoren (11) und gewinnt so eine gewisse Immunität gegenüber der zerstörerischen Wirkung hochkonzentrierter gelöster Substanzen.
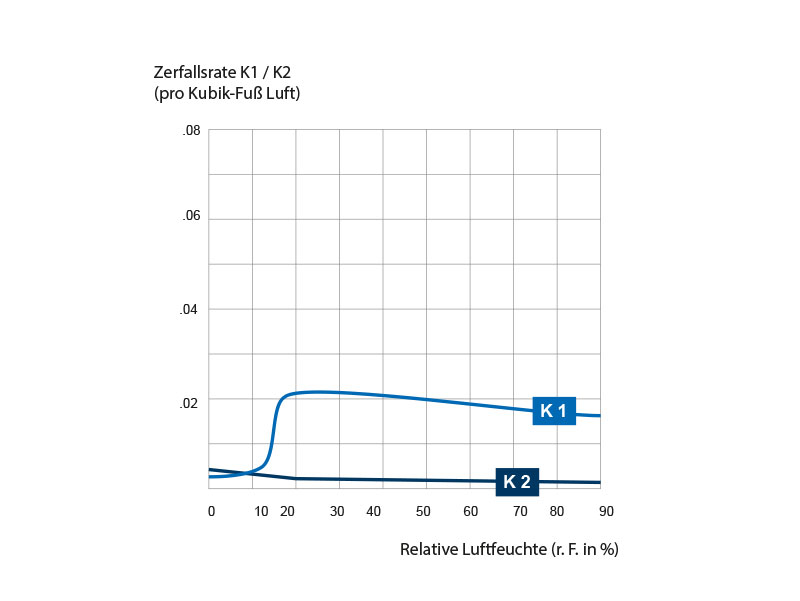
Steigungen der Absetzkurven von Tröpfchen aus einer Wolke von 3,2 µm, eingebracht in Atmosphären mit verschiedenen relativen Luftfeuchtigkeiten. K1 ist die Steigung des ersten Teils der Kurve und K2 die logarithmische Zerfallskonstante für den letzten Abschnitt. Der Unterschied zwischen dieser Kurve und der aus Abb. 2 zeigt, dass die gesteigerte Rate des Verschwindens lebensfähiger Mikroorganismen aus der Luft bei mittleren relativen Luftfeuchtigkeiten nicht durch einen Absetzprozess erklärt werden kann.
Abbildung 6
ABB. 6. Logarithmische Überlebenskonstanten von Pneumokokken, aus einer Suspension in destilliertem H2O in die Luft gesprüht, als Funktion der relativen Luftfeuchtigkeit.
Wie viel Wasser eine solche Zelle verliert, hängt von der relativen Luftfeuchtigkeit und der Bindungsenergie zwischen Wasser und den verschiedenen Bestandteilen der Zelle ab. Bei sehr niedrigen Luftfeuchtigkeitswerten ist der Wasserentzug so ausgeprägt, dass ein stabiler Zustand erreicht werden kann, in welchem der Mikroorganismus nicht durch die hohen Konzentrationen gelöster Substanzen beeinträchtigt wird.
Umgekehrt ist bei hohen relativen Luftfeuchtigkeiten ausreichend Wasser an und um die Zelle gebunden, um das Entstehen letaler Bedingungen zu vermeiden. Die hier beschriebenen Experimente deuten darauf hin, dass bei mittleren Luftfeuchtigkeitswerten die Wassermenge, die direkt mit dem Mikroorganismus assoziiert bleibt, einen kritischen Zustand in der Zelle hervorruft. In diesem Zustand wird das Bakterium sehr anfällig für die toxische Wirkung der unphysiologischen Konzentrationen gelöster Substanzen, die aus dem ursprünglichen Medium, in dem die Zellen suspendiert waren, zurückgeblieben sind.
Effekt unterschiedlicher Zusammensetzungen der Suspensionsflüssigkeit
In Anbetracht der vorangegangenen Auswertung kann angenommen werden, dass der Zuwachs der Sterberate bei mittleren Werten relativer Luftfeuchtigkeit stark reduziert werden würde, wenn die Mikroorganismen aus einer Suspension in destilliertem Wasser anstelle von Nährlösung in die Luft gesprüht würden. Diese Schlussfolgerung wurde experimentell überprüft. Siebeneinhalbstündige Kulturen von Pneumokokkus Typ I wurden zentrifugiert, einmal in destilliertem H2O gewaschen und in Wasser resuspendiert, bevor sie in die Versuchskammer gesprüht wurden. Die Überlebensrate wurde auf die übliche Weise ermittelt. Die charakteristischen linearen logarithmischen Überlebenskurven mit einem scharfen Einschnitt nach den ersten 10 oder 15 Minuten wurden exakt so beobachtet wie in den Experimenten mit Nährlösung. Anders als in letzteren Untersuchungen sorgte die Substitution von Nährlösung durch destilliertes Wasser jedoch für eine vollständige Eliminierung des starken Anstiegs der Sterberate bei Luftfeuchtigkeitswerten um 50 Prozent. Abb. 6 zeigt die Variation der logarithmischen Überlebenskonstanten von Pneumokokken, die aus Suspension in destilliertem Wasser in die Luft gesprüht wurden, mit der relativen Luftfeuchtigkeit. Ein Vergleich der Kurven aus Abb. 5 und 6 ergibt, dass das Überlebensmuster dieser luftgetragenen Pneumokokken praktisch identisch mit der Persistenz eines Aerosols aus eingefärbten Tröpfchen ist, was die Abwesenheit letaler Prozesse andeutet.
Es stellte sich die Frage, welche der Komponenten der Nährlösung die toxischen Effekte ausübte, die bei relativen Luftfeuchtigkeiten um 50 Prozent beobachtet wurden. Zu ihrer Beantwortung wurden separate Lösungen der verschiedenen Komponenten der Nährlösung hergestellt. Die Lösung jeder Komponente wurde in der gleichen Konzentration angesetzt, wie sie in der Standard-Nährlösung vorliegt, und als Suspensionsmedium verwendet, aus welchem Pneumokokken in die Luft gesprüht wurden. Diese Experimente ergaben, dass NaCl, in der Ursprungslösung in einer Konzentration von 0,5 Prozent vorliegend, zum größten Teil für die letale Wirkung verantwortlich war. Keiner der anderen Bestandteile der Nährlösung, ob einzeln oder in Kombination getestet, konnte einen letalen Effekt bei mittleren relativen Luftfeuchtigkeiten hervorrufen. Die Bestimmung der Überlebenskonstanten von Pneumokokkus-Kulturen, die aus einer Suspension mit allen Komponenten außer NaCl in die Luft gesprüht wurden5, ergab ein Kurvenpaar vergleichbar mit dem in Abbildung 6.
Wenn dagegen eine Lösung mit ausschließlich 0,5 Prozent NaCl verwendet wurde, ergaben sich Überlebenskurven wie in Abbildung 2. Der charakteristische rapide Anstieg der Sterblichkeitsrate bei mittleren relativen Luftfeuchtigkeiten tritt demnach nur in Gegenwart von NaCl auf.
Vor dem Hintergrund dieser Ergebnisse war es wichtig, den Effekt der relativen Luftfeuchtigkeit auf Bakterien zu untersuchen, die aus einer Suspension in Speichel in die Luft gesprüht wurden. Diese Flüssigkeit stellt das natürliche Medium dar, aus welchem respiratorische Bakterien in die Umgebungsluft eingebracht werden, sodass das Überlebensmuster der darin suspendierten Mikroorganismen direkt mit den Problemen natürlicher aerogener Infektionen in Verbindung gebracht werden kann. Speichel wurde von menschlichen Freiwilligen gesammelt, die zuvor für einige Minuten Paraffin gekaut hatten, um den Speichelfluss anzuregen. Es wurde nicht versucht, die Flüssigkeit von ihrer normalen Bakterienpopulation zu befreien, da diese Mikroorganismen in der finalen Suspension im Verhältnis zu den Pneumokokken in so geringer Zahl vorhanden waren, dass sie eine vernachlässigbare Kontaminierung darstellten. Eine siebeneinhalbstündige Kultur von Pneumokokken Typ I wurde zentrifugiert und in einem identischen Volumen Speichel resuspendiert. Die sich ergebende Suspension wurde sofort in den Zerstäuber transferiert und unter Anwendung des üblichen Verfahrens, wie in den vorangegangenen Experimenten beschrieben, in die Kammer gesprüht. Das resultierende Überlebensmuster war vergleichbar mit dem, welches bei Verwendung von Nähr- oder Salzlösung (Abb. 2) als Suspensionsmedium erhalten wurde, nicht aber mit der Kurve, die aus der Verwendung destillierten Wassers resultierte (Abb. 6).
Effekt der Tröpfchengröße
Wenn das Sterben der aus einer Suspension im Nährmedium oder Speichel in die Luft gesprühten Bakterien tatsächlich in Zusammenhang mit einem Dehydratisierungsprozess steht, dann sollte eine relative Luftfeuchtigkeit, die normalerweise letal wirkt, diesen Effekt in wesentlich schwächerer Ausprägung hervorrufen, wenn die Bakterien in kleinen Tröpfchen suspendiert werden statt in größeren. Diese Folgerung lässt sich ziehen, da das kleinere Tröpfchen auch eine geringere Menge der schädlichen Substanzen enthält und damit der Mikroorganismus bei fortschreitender Dehydratisierung einer geringeren Konzentration ausgesetzt ist. Dieser Effekt wurde durch den Vergleich der Überlebensraten von Pneumokokken, die aus einer Suspension in Serum-Dextrose-Nährlösung in die Luft gesprüht wurden, bei Verwendung zweier verschiedener Zerstäuber untersucht, deren Partikelgrößenverteilungen medianen Massendurchmessern von 1,6 µm bzw. 3,2 µm entsprachen.
In Abb. 7 ist eine typische Versuchsreihe bei 22,2°C und 50 Prozent relativer Luftfeuchtigkeit dargestellt, die demonstriert, dass die Sterberate für in größeren Tröpfchen suspendierte Pneumokokken höher liegt. In einer Reihe aus mehr als 15 Experimenten bei 22,2°C lag der durchschnittliche Wert der Zerfallskontante K1, die während der ersten 10 bis 20 Minuten nach Beendigung des Sprühvorgangs beobachtet wird, für Partikel von 1,6 µm Durchmesser bei 0,012 ± 0,005 pro Minute und für Partikel von 3,2 µm Durchmesser bei 0,32 ± 0,12 pro Minute. Der durchschnittliche Wert für K2, die Sterberate im zweiten Abschnitt der Überlebenskurve, lag für die Partikel von 1,6 µm bei 0,045 pro Minute. (Für die Partikel von 3,2 µm hatten nach den ersten 20 Minuten nur so wenige Bakterien überlebt, dass kein zufriedenstellender Wert für K2 bei 50 Prozent relativer Luftfeuchtigkeit ermittelt werden konnte.)
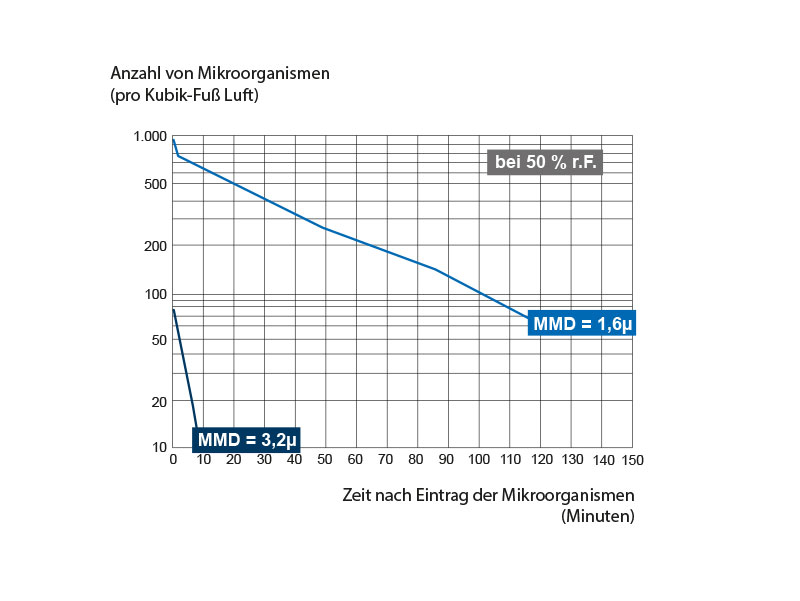
Effekt der Partikelgröße in der Wolke auf das Überleben von Pneumokokken, die aus der Suspension in der Nährlösung in eine Atmosphäre von 50 Prozent relativer Luftfeuchtigkeit bei 22,2°C gesprüht werden.
Effekt der Temperatur auf die Überlebenskonstanten von Pneumokokken, die aus der Suspension in der Nährlösung in Atmosphären mit verschiedenen relativen Luftfeuchtigkeiten gesprüht werden.
Einfluss der Temperatur
Die Auswirkungen von Temperaturveränderungen auf diesen letalen Prozess wurden ebenfalls untersucht. Das Überleben von Pneumokokken aus Suspensionen in der Nährlösung, die bei verschiedenen Werten relativer Luftfeuchtigkeit in die Luft gesprüht wurden, wurde bei 14,4°C und bei 33,3°C sowie bei 22,2°C gemessen.Wie zu erwarten, wurde ein ausgeprägter Temperaturkoeffizient beobachtet; K1 variierte zwischen diesen Temperaturextremen um einen Faktor von fünfzehn. In Abb. 8 sind die Werte von K1 und K2 als Funktion der relativen Luftfeuchtigkeit bei den drei Temperaturen dargestellt. Wie schon zuvor sind die Werte für K2 bei mittleren Luftfeuchtigkeiten für die zwei höheren Temperaturen ungenau, da durch die extrem hohen anfänglichen Sterberaten unter diesen Bedingungen zu wenige überlebende Organismen für eine Untersuchung des anschließenden letalen Prozesses zurückbleiben.
Diskussion
Wenn eine Suspension einer gegebenen Zusammensetzung in die Atmosphäre zerstäubt wird, hängt der letztendliche Grad der Dehydratisierung von der relativen Luftfeuchtigkeit ab, da das Tröpfchen schließlich in einen Zustand des Gleichgewichts mit der Atmosphäre übergeht. Wenn dieser eintritt, hat das Partikel einen Wassergehalt, der eine Oberflächenspannung erzeugt, die identisch mit dem Wasserpartialdruck in der Luft ist. Bei niedrigen relativen Luftfeuchtigkeiten wird ein Partikel, das einen Mikroorganismus enthält, somit fast sein gesamtes Wasser verloren haben, wovon ein Teil sogar in fester chemischer Verbindung mit bestimmten zellulären Bestandteilen gestanden haben könnte. Bei hohen relativen Luftfeuchtigkeiten dagegen bleibt selbst nur lose gebundenes Wasser erhalten. Bei mittleren relativen Luftfeuchtigkeiten tritt eine partielle Dehydratisierung der verschiedenen zellulären Systeme auf. Berechnungen zeigen, dass kugelförmige Tröpfchen destillierten Wassers selbst bei einer relativen Luftfeuchtigkeit von 50 Prozent von einem ursprünglichen Durchmesser von 3 µm innerhalb von 0,004 Sekunden auf ein Zehntel dieser Größe verdampfen können.6 Das ist wesentlich schneller als jede der in den hier präsentierten Experimenten beobachteten Sterberaten, sodass der Verdampfungsprozess abgeschlossen wäre, bevor der letale Prozess auch nur beginnen könnte. Dementsprechend müssen die in diesen Experimenten beobachteten Mortalitätsraten als Repräsentation der natürlichen Sterblichkeit der Mikroorganismen in einer gegebenen chemischen Umgebung interpretiert werden, bei einem Hydratisierungsgrad, der mit der vorherrschenden relativen Luftfeuchtigkeit im Gleichgewicht steht.
Wenn die hier vorgeschlagene theoretische Formulierung korrekt ist, ist die Salzaktivität nicht allein verantwortlich für die bei mittleren Luftfeuchtigkeiten beobachtete letale Wirkung. In die Luft gesprühte Tröpfchen reiner Natriumchloridlösung sind bei einer relativen Luftfeuchtigkeit von 75 Prozent mit dieser Substanz gesättigt (13) und würden bei niedrigeren Luftfeuchtigkeiten vollständig austrocknen. In unseren Experimenten allerdings zeigte sich für in reiner Kochsalzlösung suspendierte Mikroorganismen ein maximaler letaler Effekt bei relativen Luftfeuchtigkeiten um 50 Prozent, nicht 75 Prozent. Diese scheinbare Diskrepanz lässt sich damit erklären, dass das Salz in einer bakteriellen Suspension mit einigen zellulären Bestandteilen in Lösung geht und Verbindungen eingeht. Die maximale letale Wirkung des in der Zelle gebundenen Salzes entfaltet sich bei der relativen Luftfeuchtigkeit, die den Mikroorganismus so weit austrocknet, dass er am verwundbarsten ist, nicht bei einer Luftfeuchtigkeit, in der ein Gleichgewicht mit einer gesättigten Lösung von reinem NaCl vorliegt.
Die vorliegenden Untersuchungsergebnisse wurden erklärt durch die Postulierung der Existenz eines kritischen Feuchtigkeitsgehalts, bei welchem eine bakterielle Zelle wesentlich anfälliger für toxische Substanzen wird, als sie es bei einem höheren oder niedrigeren Wassergehalt wäre. Weitere Anhaltspunkte deuten darauf hin, dass dieses Phänomen charakteristisch für bakterielle Systeme ist. Dieses Prinzip liegt dem Lyophilisierungsprozess zur Trocknung lebensfähiger Mikroorganismen zugrunde. Wird bakteriellen Zellen bei Raumtemperatur Wasser entzogen, so stirbt die Kultur sehr schnell ab. Um das zu vermeiden, werden die Bakterien zunächst auf eine Temperatur abgekühlt, die so niedrig ist, dass die Rate des letalen Prozesses stark reduziert wird. Dann wird das Wasser so rasch wie möglich entzogen. Nachdem die Zellen so weit dehydratisiert wurden, dass der kritische Bereich verlassen wurde, können sie erneut auf Raumtemperatur gebracht werden, ohne eine ausgeprägte Sterblichkeit aufzuweisen. Die Anwendung dieser Überlegungen hat die Entwicklung einer simplen Methode zur Trocknung von Mikroorganismen ermöglicht, ohne auf die niedrigen Temperaturen zurückgreifen zu müssen, die beim Lyophilisierungsprozess zum Einsatz kommen. Es hat sich gezeigt, dass Zellen ohne Beeinträchtigung der Überlebensfähigkeit bei Raumtemperatur dehydratisiert werden können, solange die Trocknung so schnell vonstattengeht, dass der stabile Zustand erreicht wird, bevor die letalen Prozesse ihre Wirkung entfalten können. Diese Studien werden in einer in Kürze erscheinenden Publikation beschrieben (14). Die wesentlich größere Effizienz von Dampfsterilisation im Vergleich mit Erhitzungsprozessen bei Trockenheit beruht zweifellos auf demselben Phänomen.
Mikroorganismen, die in der Gegenwart von Dampf erhitzt werden, verbleiben in einem Zustand mittlerer Hydratisierung, was sie für die tödliche Wirkung der hohen Temperaturen anfälliger macht, als sie es in vollständig ausgetrocknetem Zustand wären. Ein weiteres Beispiel für die Funktionsweise dieses Effekts findet sich in der verminderten Effektivität der Eliminierung von Luftkeimen durch aerosolartige Desinfektionsmittel wie Glykole bei niedrigen relativen Luftfeuchtigkeiten (5, 6). Dieser Effekt beruht zum Teil darauf, dass der germizide Dampf auf getrockneten Partikeln, die entstehen, wenn eine bakterielle Wolke in einer sehr trockenen Umgebungsluft verteilt wird, weniger gut kondensiert. Aktuelle Experimente in vitro haben jedoch auch gezeigt, dass vollständig getrocknete Bakterien resistenter gegenüber der letalen Wirkung von Glykolen im flüssigen Zustand sind (15).
Die Werte für K1 und K2, wie sie hier berechnet wurden, repräsentieren die logarithmischen Raten der Entfernung lebensfähiger Bakterien aus der Atmosphäre und enthalten damit sowohl die Absetzraten als auch die letalen Prozesse durch die Präsenz von NaCl bei kritischen Luftfeuchtigkeitswerten. Werden die entsprechenden Absetzraten aus Abb. 5 von diesen abgezogen, ergeben sich für die Sterblichkeitsraten aller drei hier untersuchten Mikroorganismen sowohl bei sehr niedrigen als auch bei sehr hohen relativen Luftfeuchtigkeiten extrem kleine Werte. In einigen Fällen ist das Ergebnis negativ, was lediglich bedeutet, dass die Sterberate zu klein ist, um mit dieser Technik genau evaluiert werden zu können.
Die vom NaCl ausgehende letale Wirkung bei einem kritischen Grad zellulärer Dehydratisierung beruht vermutlich unter anderem auf der Denaturierung eines oder mehrerer lebenswichtiger Enzymsysteme. Weitere Untersuchungen des Mechanismus dieses letalen Prozesses und des Verhaltens der Bakterienzellen in verschiedenen Hydratationszuständen sind in Arbeit.
Für eine Evaluation der Signifikanz der hier berichteten Ergebnisse für epidemiologische Probleme bedarf es weiterer Studien. Dafür werden ausführlichere Untersuchungen des Verhaltens einer größeren Zahl von Pathogenen erforderlich sein, insbesondere in der Gruppe der Viren. Möglicherweise können diese Effekte auch bei der Erklärung einiger Aspekte der saisonal auftretenden Verbreitung einiger Atemwegserkrankungen helfen. Es ist auch möglich, dass mit der Feuchtigkeitsregulierung selbst ein gewisser Effekt als prophylaktische Maßnahme erzielt werden kann. Vorläufige Experimente haben ergeben, dass durch das Einbringen einer sorgsam regulierten Menge an Dampf in die Luft einer Kammer eine luftgebundene Dispersion von Pneumokokken, die für eine Stunde in einer sehr trockenen Atmosphäre ausgetrocknet worden waren, rehydriert und rapide abgetötet werden kann. Obwohl ein Erhöhen der relativen Luftfeuchtigkeit auf über 50 Prozent die Kontamination mit Luftkeimen nicht so effektiv verringern kann wie Glykoldampf oder UV-Strahlung, würde die Einfachheit dieser Maßnahme ihren Einsatz in einer Vielzahl von Situationen empfehlen, wenn sie auch nur einen teilweise förderlichen Effekt hätte.
Zusammenfassung
Es wurde die Überlebensfähigkeit von Pneumokokkus Typ I, der aus einer flüssigen Suspension in die Atmosphäre gesprüht wurde, als Funktion der relativen Luftfeuchtigkeit gemessen. Bei Verwendung von einer Nährlösung, Speichel oder 0,5-prozentiger Kochsalzlösung als Suspensionsmedium werden bei relativen Luftfeuchtigkeiten um 50 Prozent sehr hohe Sterblichkeitsraten observiert. Bei Luftfeuchtigkeiten über oder unter diesem Wert überleben die Mikroorganismen jedoch über längere Zeiträume.Durch Messung der Absetzrate der in diesen Experimenten eingesetzten Tröpfchen wurde demonstriert, dass das Verschwinden der Mikroorganismen aus der Luft in der Tat einen letalen Prozess dargestellt, nicht nur eine Manifestation von Kollisionsprozessen. Bei Verwendung einer salzfreien Lösung verschwindet der bei mittleren relativen Luftfeuchtigkeiten beobachtete deutliche Spitzenwert der Sterberate. Der letale Effekt mittlerer relativer Luftfeuchtigkeiten auf Pneumokokken, die aus einer salzhaltigen Suspension zerstäubt wurden, vergrößert sich, wenn die Partikelgröße der zerstäubten Tröpfchen gesteigert oder wenn die Temperatur erhöht wird.
Kulturen von hämolytischem Streptokokkus Gruppe C und Staphylokokkus, ebenfalls aus einem Nährmedium zerstäubt, zeigen das gleiche allgemeine Überlebensmuster als Funktion der relativen Luftfeuchtigkeit, obwohl die Sterblichkeitsraten kleiner sind als bei Pneumokokkus.
Diese Effekte können mit der Annahme der Existenz eines kritischen Grades zellulärer Dehydratisierung erklärt werden, bei dem die Mikroorganismen wesentlich anfälliger für toxische Substanzen werden, als sie es sind, wenn mehr oder weniger Wasser an die Zelle gebunden ist.
Die hier dargestellten Ergebnisse könnten für die Erklärung bestimmter Aspekte der Epidemiologie von Tröpfcheninfektionen von wesentlicher Bedeutung sein.
1 Für alle hier beschriebenen Experimente wurde der gleiche Zerstäuber verwendet, abgesehen von den Fällen, in denen der Effekt verschiedener Partikelgrößen untersucht wurde.
2 Das heißt, 50 Prozent der Masse der Wolke war in Tröpfchen mit einem Durchmesser von weniger als 3,2 µm enthalten.
3 Sie ist besonders niedrig bei einer relativen Luftfeuchtigkeit unter 12 Prozent. Der scharfe Einschnitt in der Kurve an diesem Punkt würde bedeuten, dass bei dieser relativen Luftfeuchtigkeit die vollständige Entfeuchtung der Partikel erfolgt.
4 Diese Daten zum Absetzen weisen auch darauf hin, dass die schnellere Rate des Verschwindens einer bakteriellen Suspension während der ersten 10 bis 20 Minuten nach Zerstäubung (also der Unterschied zwischen K1 und K2) durch Prozesse verursacht wird, die selektiv größere Partikel stärker beeinträchtigen als kleinere. Das Absetzen der größeren Partikel aus der Wolke in den ersten 10 bis 15 Minuten ist zweifelsfrei für die gesteigerte anfängliche Rate des Verschwindens des gefärbten Aerosols verantwortlich. Der gleiche Prozess, kombiniert mit jedem Einfluss, den die höhere Partikelgröße per se auf die Beschleunigung des Absterbens von in den Tröpfchen enthaltenen Bakterien haben könnte, würde die Existenz zweier separater Sterberaten belegen, K1 und K2, die typischerweise beobachtet werden, wenn eine Wolke aus Bakterien enthaltenden Tröpfchen unter den hier beschriebenen Bedingungen in die Atmosphäre eingebracht wird (siehe unten, Abschnitt über Partikelgröße).
5 Das heißt, diese Lösung enthielt 1 Prozent Pepton, 1 Prozent Tryptose, 0,05 Prozent Dextrose und 2,0 Prozent Serum.
6 Wie bereits gezeigt wurde (12), verläuft die Verdampfungsrate kleiner Tröpfchen in ungesättigter Luft entsprechend der folgenden Gleichung: dA/dt= 8πDM/RTd(ρ_g-〖ρ'〗_g) wobei A = Fläche des Tröpfchens, D = Dampfdiffusionskoeffizient, für Wasserdampf in der Luft bei Raumtemperatur gleich 0,24 cm2 pro Sekunde; M = Molekulargewicht des Dampfes, 18,0 für H20; R = Gaskonstante, 62 400 cc. x mm. Hg. mol-1 deg.-1; T = absolute Temperatur, 296° A; d = Dichte des verflüssigten Dampfes, was die Einheit für Wasser ist; ρg = Teildruck des Wasserdampfes in der Atmosphäre, der dem Produkt der relativen Luftfeuchtigkeit und des Dampfdrucks von Wasser bei der Temperatur des Experiments entsprechen würde; und ρ'g = Druck des Wasserdampfes im Gleichgewicht mit dem Tröpfchen.
Für Tröpfchen reinen Wassers würde ρ‘ dem reinen Dampfdruck entsprechen, der bei 22,2°C bei 20,1 mm Hg. liegt. Wenn das Tröpfchen andere in der wässrigen Phase gelöste Substanzen enthält, würde ρ‘ um den Anteil reduziert werden, der der Verringerung des Dampfdrucks durch die Kombination der gelösten Substanzen entspricht. Das Vorliegen von Salzen und Proteinen in den Tröpfchen würde die Verdampfungsrate etwas verringern, aber nicht einmal eine gesättigte Salzlösung könnte den Dampfdruck in einem Maß senken, das ausreichend wäre, um die Verdampfungsrate signifikant zu verringern.
Diese Arbeit wurde unterstützt vom United States Public Health Service, dem Bartlett Memorial Fund of the University of Chicago und der Carbide and Carbon Chemicals Corporation. Vorgelegt bei der Graduate School of the University of Chicago in teilweiser Erfüllung der Anforderungen für den akademischen Grad Master of Science (Edward W. Dunklin).
Dr. med. Walter J. Hugentobler
Die untersuchten Bakterien wurden in der Luft schnell inaktiviert, wenn sie Luft mit einer relativen Luftfeuchtigkeit von etwa 50% ausgesetzt wurden. Dies zeigt offensichtlich die Schutzwirkung einer mittleren Luftfeuchtigkeit.
Dass keine Inaktivierung zu beobachten war, wenn die Bakterien nur in Wasser versprüht wurden, im Gegensatz zu Versprühung mit Salzlösungen oder Speichel zeigt, dass Bestandteile, die in den Tröpfchen enthalten sind, eine wichtige Rolle bei der Inaktivierung der Bakterien spielen.
Zum Zeitpunkt der Untersuchung war eine ganze Generation von Forschern aus den Bereichen Mikrobiologie, infektiöse Aerosole und Luftübertragung davon überzeugt, dass die Ergebnisse von Dunklin und Puck weitreichende Konsequenzen hinsichtlich der Kontrolle und Verhinderung der Ausbreitung von Infektionskrankheiten in der Luft haben würden. Leider wurden ihre Forschungsergebnisse bis vor kurzem nicht wissenschaftlich weiter verfolgt und die Ergebnisse hatten nur geringe Auswirkungen auf die Gestaltung der Gebäudetechnik.
Quellen
Originaltitel: The leathal effect of relative humidity on air-borne bacteria
Quellenlink: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2135764/
Veröffentlicht: 01.10.1947
1. Williamson, A. E., and Gotaas, H. B., Ind. Med., 1942, 11, Ind. Hyg. Sect. 3, 40.
2. Edwards, D. G. ft., Elford, W. J., and Laidlaw, P., J. ttyg., 1943, 43, 1. Loosli, C. G., Lemon, H. M., Robertson, O. H., and Appel, E., Prec. Sec. Exp. Biol. and Med., 1943, 83, 205.
3. DeOme, K. B., and Personnel of Naval Laboratory Research Unit No. 1, Am. J. Hyg., 1944, 40, 239.
4. Wells, W. F., and Zappasodi, P., Science, 1942, 96, 277.
5. Puck, T. T., Robertson, O. H., and Lemon, H. M., J. Exp. Med., 1943, 78, 387.
6. Puck, T. T., J. Exp. Med., 1947, 85, 729; 1947, 85, 744.
7. Robertson, O. H., Puck, T. T., and Wise, H., J. Exp. Med., 1946, 84, 559.
8. Graeser, J. B., and Rowe, A. H., Am. J. Dis. Child., 1936, 52, 92.
9. May, K. R., J. Scient. Instr., 1945, 9.2, 187.
10. Lemon, H. M., Prec. Soc. Exp. Biol. and Med., 1943, 54, 298.
11. Porter, J. R., Bacterial Chemistry and Physiology, New York, John Wiley and Sons, 1946, 195.
12. Langmiur, I., Physic. Rev., 1918, 129 368.
13. Intemational Critical Tables, New York, McGraw-Hill Book Co., Inc., 1928, 3, 369.
14. Puck, T. T., and Dunklin, E., data to be published.
15. Robertson, O. H., et al., data to be published.
Studie Ajit Ahlawat
Die Übertragung des schweren akuten respiratorischen Syndroms Coronavirus 2 (SARS-CoV-2) durch die Luft wurde als potenzielle Pandemieherausforderung...
Einfluss der Luftfeuchte auf Mensch und Gesundheit
In der wissenschaftlichen Literatur werden unterschiedliche Empfehlungen für untere und obere Grenzwerte der relativen Luftfeuchte für Innenräume gen...
Auswirkungen von Umweltfaktoren auf COVID-19
Auswirkungen von Umweltfaktoren auf den Schweregrad und die Sterblichkeitsquote von COVID-19.
Saisonalität der respiratorischen viralen Infektionen
Der saisonale Zyklus von respiratorischen Virusinfektionen ist seit Tausenden von Jahren bekannt. Jahr für Jahr wird die Bevölkerung der gemäßigten K...
Luftfeuchtigkeit in Schulklassen
Influenza ist ein globales Problem und betrifft jährlich 5–10 % der Erwachsenen und 20–30 % der Kinder. Nicht-pharmazeutische Interventionen (NPIs) s...
COVID-19: Reduzierung der Übertragung
Aufgrund der weltweit zunehmenden Infektionen mit dem schweren akuten respiratorischen Coronavirus-2-Syndrom (SARS-CoV-2), das die Coronavirus-Krankh...
Überlebensfähigkeit von Coronaviren
In dieser Studie wurden die Auswirkungen der Lufttemperatur und der relativen Luftfeuchtigkeit auf das Überleben von Coronaviren auf Oberflächen unte...
Optimale Raumluftfeuchte
Optimale Luftfeuchte in Räumen ist notwendig, um das Wohlbefinden des Menschen zu steigern, aber im Gegensatz zu den meisten anderen Schadstoffen in ...
Auswirkung auf das Sick-Building-Syndrom
Das Ziel dieser Studie war die wissenschaftliche Auseinandersetzung der Auswirkungen von Dampfluftbefeuchtung auf das Sick-Building-Syndroms (SBS) un...
Das saisonale Auftreten von Influenza Viren
Die im Winter beobachtete gesteigerte Sterblichkeit in gemäßigten Zonen wird zu großen Teilen der saisonalen Influenza zugeschrieben. Eine Reanalyse ...